Si tienes más de 50 años, probablemente tengas al menos un diente perdido o un implante. Por una buena razón: los dientes no se regeneran después de dañarse. Ni en el reino animal, ni en nosotros. Un diente de leche se cae, un diente adulto crece debajo. Pero después de que el diente permanente se va, se acabó. Hasta ahora. En un nuevo estudio publicado en el International Journal of Oral Science en enero de 2026, un equipo de la Universidad de Sichuan en China identificó una proteína llamada SMAD7 como un interruptor molecular que puede activar las células madre en los dientes. Si este enfoque funciona en la clínica, cambiará la odontología desde sus cimientos.
El problema: ¿Por qué los dientes no se regeneran?
Las membranas mucosas de tu intestino se regeneran cada 4-5 días. Tu piel, cada mes. El hueso, cada 10 años. Pero ¿un diente? Nunca se regenera. ¿Por qué?
La razón: los dientes están compuestos por 3 tejidos:
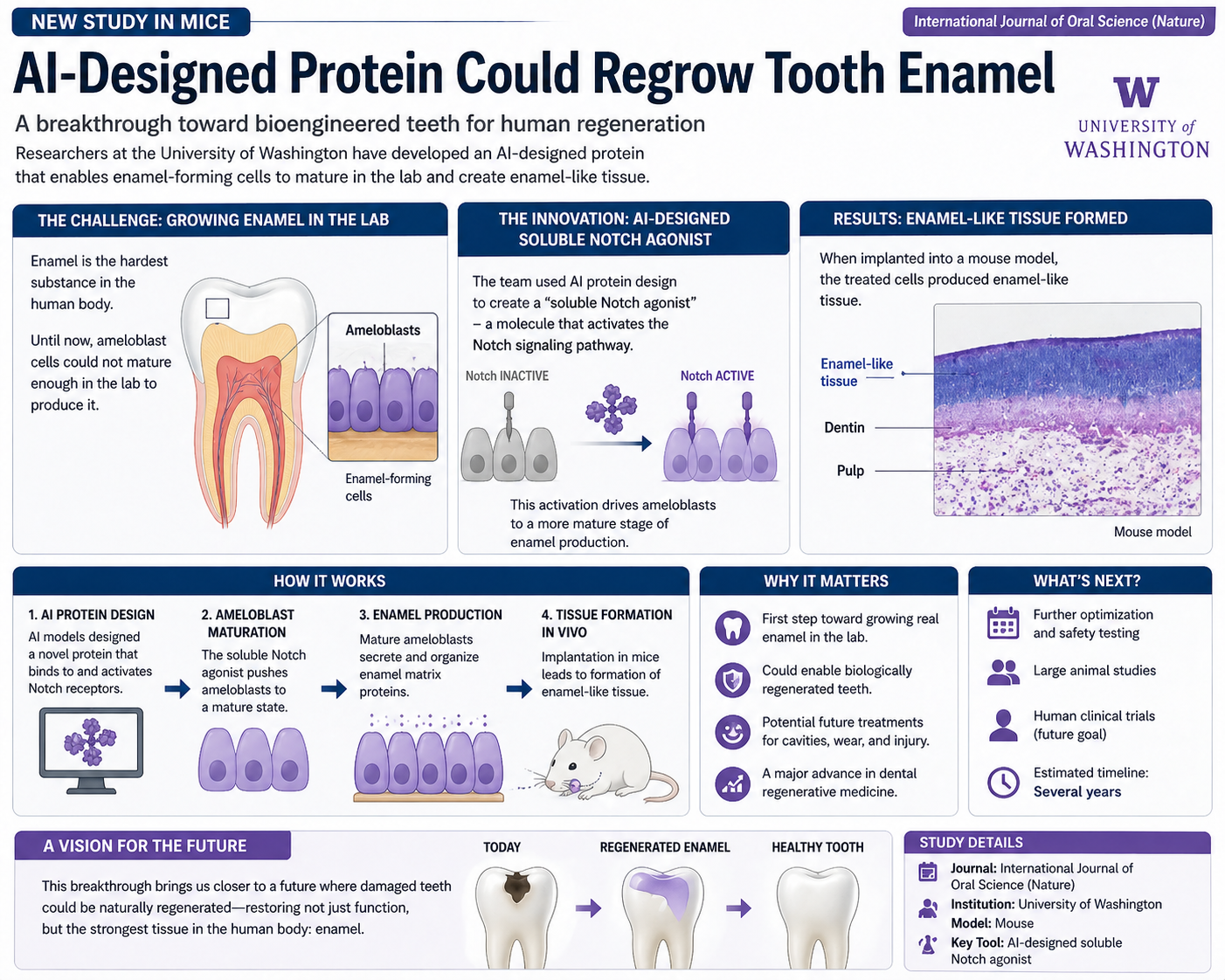
- Esmalte: la capa externa dura. No tiene células. No hay nada que regenerar.
- Dentina: la capa media. Tiene células, pero pocas.
- Pulpa (nervio del diente): la capa interna. Contiene células madre.
Si el daño al diente es leve, las células de la pulpa pueden producir un poco de dentina secundaria. Pero son muy limitadas. Daño grande: simplemente no pueden construir un diente nuevo.
Esto es diferente a los tiburones, que reemplazan sus dientes constantemente. ¿Qué es diferente en ellos? Las vías de las células madre están siempre activas.
El descubrimiento: SMAD7 como interruptor
El equipo liderado por el Dr. Tian Chen del Hospital West China de Estomatología estudió células madre en la pulpa dental humana. Se preguntaron: ¿Qué permite o impide que se dividan para construir tejido nuevo?
En una serie de experimentos, identificaron el papel crítico de SMAD7, una proteína que hasta ahora se consideraba un componente secundario. Ahora se sabe: SMAD7 es un interruptor principal.
¿Cómo funciona SMAD7?
En condiciones normales, hay dos vías que dirigen las células madre en el diente:
- TGF-β / SMAD2/3: la vía "deja de dividirte". Activa protección pero también ralentiza.
- Wnt / β-catenina: la vía "divídetey regenérate". Estimula la producción.
Ambas vías están en conflicto. Cuando una está activa, la otra está suprimida. SMAD7 es el árbitro: cuando SMAD7 está activo, suprime TGF-β y libera β-catenina para activar Wnt. Las células madre comienzan a dividirse y construir.
Sin suficiente SMAD7 activo:
- TGF-β/SMAD2/3 domina
- Atrapa β-catenina y le impide actuar
- Las células madre entran en modo "detente"
- No hay renovación
Descubrimiento innovador: SMAD7 como socio directo
El hallazgo más sorprendente: SMAD7 no solo permite que Wnt funcione, sino que es un socio directo. Se une físicamente a β-catenina y juntos actúan sobre genes que activan las células. Este es un mecanismo previamente desconocido.
Esto también significa: si encontramos una manera de aumentar SMAD7, podremos activar la regeneración dental en cualquier momento y lugar.
¿Qué significa esto en la práctica?
El equipo ve varias aplicaciones posibles:
1. Mejora de los tratamientos de conducto
Los tratamientos de conducto estándar eliminan la pulpa (el nervio) y la reemplazan con material inerte. Esto vuelve al diente "muerto" pero salva la cubierta. Con SMAD7, quizás se pueda salvar la pulpa y promover su regeneración.
2. Reparación del daño a la dentina
Caries, desgaste. En lugar de restaurar con un empaste, es posible que el diente mismo pueda repararse.
3. Implante autólogo cultivado
En un futuro más lejano: se podrían tomar algunas células madre de tu boca, potenciarlas con SMAD7 e implantarlas en el lugar de un diente perdido. Construirían un diente completamente nuevo a partir de tu propio sistema.
4. Tratamientos contra la inflamación de las encías
La inflamación avanzada de las encías lleva a la pérdida de hueso y dientes. SMAD7 podría ayudar en la regeneración del hueso y los tejidos de soporte.
Los próximos pasos
El equipo ahora está en investigación avanzada:
- Desarrollo de compuestos que activen SMAD7: moléculas pequeñas, anticuerpos
- Pruebas en ratones: verificación de seguridad y eficacia
- Pruebas en perros: sus dientes son más similares a los humanos
- Pruebas en humanos: se esperan 5-7 años
Inicialmente, los tratamientos serán para casos específicos (después de tratamientos de conducto, daño en encías), y luego se ampliarán.
Lo que puede ayudar ahora (tratamiento no basado en SMAD7)
Incluso sin el nuevo tratamiento, hay formas de apoyar la salud de las células madre en los dientes:
1. Vitamina D y K2
Esenciales para la salud dental y ósea. La K2 específicamente ayuda a la mineralización.
2. Evitar azúcares procesados
Dos razones: causan caries y también reducen la actividad de las células madre en general.
3. Dieta rica en polifenoles
Té verde, cúrcuma, cacao: los polifenoles apoyan la actividad celular.
4. Suficiente calcio
Esencial para dientes y huesos.
5. Evitar el tabaco
De cigarrillos, azúcar y otros. Ralentiza significativamente las células madre.
Contexto más amplio
Si SMAD7 se reconoce como un interruptor general para la regeneración de tejidos, podría ser relevante también para:
- Regeneración ósea (osteoporosis)
- Regeneración de colágeno en la piel
- Regeneración de cartílago en las articulaciones
- Regeneración de tejidos después de lesiones
Esto es lo que hace importante esta investigación. No solo se trata de dientes, sino del mecanismo básico de la regeneración de tejidos.
La conclusión final
Que los dientes vuelvan a crecer ya no es ciencia ficción. En 2030 lo probaremos en humanos. En 2035 quizás esté disponible como primer tratamiento. Hasta entonces, cuida los dientes que tienes: siguen siendo los mejores. Pero si pierdes un diente en 2030, es posible que escuches al médico: "¿Prefieres un implante o que se regenere de forma natural?"

💬 תגובות (0)
היו הראשונים להגיב על המאמר.