הסיפור של רפואת ההשתלות הוא אחד הסיפורים היפים והכואבים ביותר של הרפואה המודרנית. ב-1954 ניתחו שני אחים תאומים בבוסטון, ולאחד מהם הושתלה כליה מאחיו. זו הייתה ההשתלה המוצלחת הראשונה אי-פעם, ופתחה עידן חדש שבו אפשר להחליף איבר מקולקל באיבר עובד. מאז, מיליוני אנשים קיבלו חיים שניים: כליות, כבדים, לבבות, ריאות, לבלבים, כל אחד נלקח מאדם אחר, מת או חי, והושתל בגוף שזקוק לו.
אבל יש בעיה מבנית בסיפור הזה. תורמים הם משאב מוגבל מאוד, וקיים פער דרמטי בין הביקוש להיצע. בקנדה לבדה, רשימת ההמתנה לאיברים מונה היום מעל 4,400 איש, וכ-250 מהם מתים מדי שנה לפני שמתפנה תורם מתאים. בארה"ב המספרים גדולים פי 25: יותר מ-100,000 בהמתנה, וכ-17 מתים בכל יום. בישראל, יותר מ-1,200 איש נמצאים ברשימה, ורק כ-450 השתלות מתבצעות בשנה.
ב-1 במאי 2026 פרסם Hospital News דיווח שמסמן רגע פנייה בסיפור הזה. מעבדת התחדשות איברים הייעודית הראשונה בעולם נפתחה בקנדה, מתקן ענק של 12,000 מטר רבוע שמטרתו לבנות איברים שלמים מתאי הגזע של המטופל עצמו, ולא להמתין לתורם. אם הגישה תעבוד, היא תהפוך את כל פרדיגמת ההשתלות על ראשה.
מה זאת בכלל התחדשות איברים?
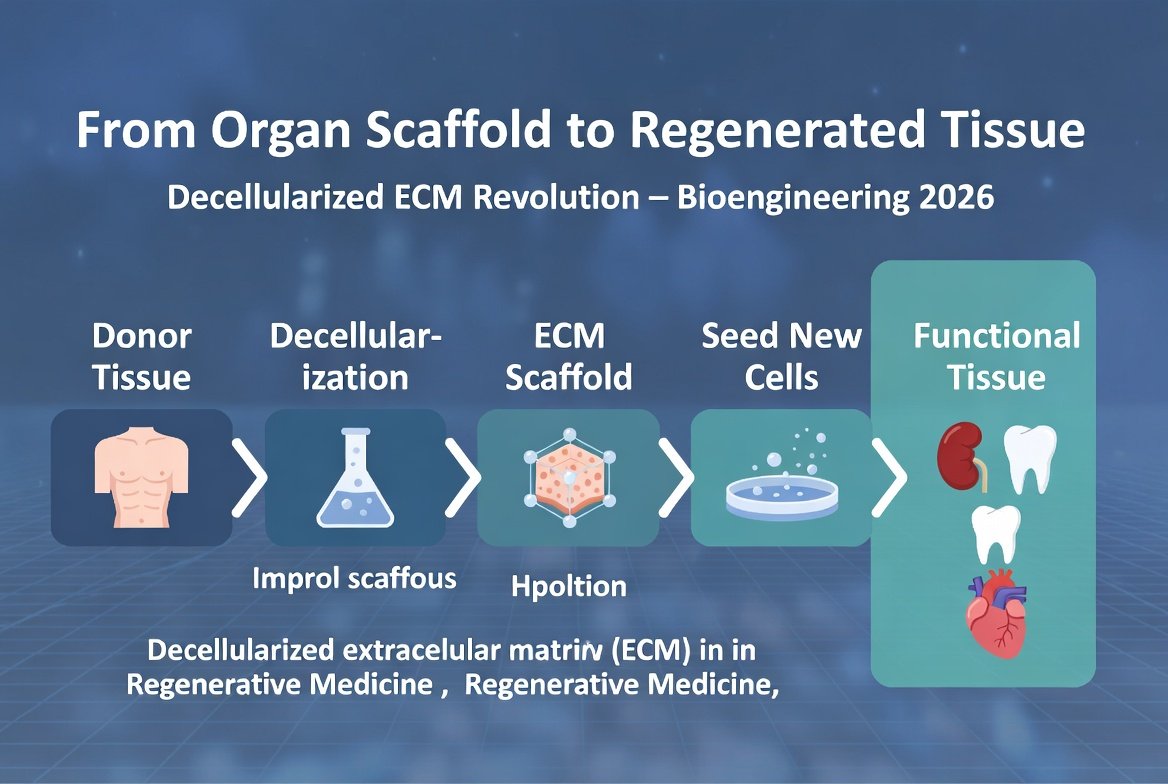
המונח regenerative medicine, רפואה רגנרטיבית, מתאר משפחה של גישות שמטרתן לגדל, לתקן או להחליף רקמה ביולוגית באמצעות תאי הגוף עצמו. התחדשות איברים שלמים היא הגביע הקדוש של התחום, ומבוססת על שלושה רכיבי ליבה:
- שלד תאי חוץ-תאי (ECM scaffold): המבנה התלת-ממדי של איבר, כולל קולגן, אלסטין, ולמינין, ללא תאים חיים. נדמה לבית ללא דיירים.
- תאי גזע אוטולוגיים: תאי גזע שמקורם במטופל עצמו, בדרך כלל מתאי גזע iPSC שתוכנתו מחדש מתאי עור או דם.
- ביוראקטור: מכשיר שמדמה תנאים פיזיולוגיים בגוף האדם, זרימת דם, לחץ, חמצן, חום, ומאפשר לתאים להתחלק ולהתבדל בתוך השלד.
- גורמי גדילה והתבדלות: סדרה של חלבונים וסיגנלים שמכוונים את התאים להפוך לרקמת לב, כליה, כבד או כל איבר שצריך.
- זמן: התהליך לוקח בין 4 ל-12 שבועות לאיבר שלם, תלוי בגודלו ובמורכבותו.
היופי של הגישה הזו הוא שהאיבר הסופי מבחינה אימונולוגית הוא חלק מהמטופל. אין צורך בתרופות חיסוניות שמדכאות את מערכת החיסון לכל החיים, אין סיכון לדחייה, ואין צורך בהתאמת רקמות. בנוסף, אין צורך בתורם, אז אין רשימת המתנה.
הגישה הזו מנוגדת לחלוטין לקסנו-טרנספלנטציה (השתלה מבעלי-חיים, בעיקר מחזירים מהונדסים גנטית), שכן בכל זאת דורשת דיכוי חיסוני, ועלולה לעורר זיהומים בין-מיניים. איבר מתאי המטופל עצמו הוא הפתרון המושלם, אם נצליח להפוך אותו לאפשרי בקנה מידה תעשייתי.
הקשר לרפואת ההשתלות: גשר על פני הפער
כדי להבין למה המעבדה הזו פורצת דרך, צריך להבין את הפער בין שני העולמות, רפואת ההשתלות הקלאסית והרפואה הרגנרטיבית.
רפואת ההשתלות בנויה על העברת איבר חי מאדם אחד לאדם אחר. היא עובדת, היא מצילה חיים, אבל היא תלויה בתורמים. בשנים האחרונות הביקוש לאיברים גדל בקצב מהיר משמעותית מההיצע, בעיקר כי האוכלוסייה מזדקנת ומקרי כשל איברים מתרחבים. ההמתנה הממוצעת לכליה בארה"ב היא 3-7 שנים, וכ-13 איש בכל יום מתים על רשימת ההמתנה לכליה לבדה.
הרפואה הרגנרטיבית, לעומת זאת, בנויה על גידול תאים ורקמות במעבדה. היא יכולה לייצר אינסוף עותקים, היא מתאימה את עצמה לכל מטופל, והיא לא דורשת תורם. הבעיה: עד היום, רק רקמות שטוחות ופשוטות הצליחו להיווצר באופן מעשי. עור, סחוס, שלפוחית שתן, כמה מקרים בודדים של קנה נשימה. איברים מורכבים כמו לב או כליה היו מעבר ליכולת הטכנולוגית.
המעבדה הקנדית החדשה מנסה לפזר את החסם הזה. היא משלבת שלוש טכנולוגיות שבכל אחת לבד הוכחה כעובדת, אבל מעולם לא שולבו יחד בקנה מידה איברי: דה-צלולריזציה (פירוק תאי), אכלוס מחדש בתאי גזע, וביוראקטור פיזיולוגי. השאלה אם אכן יעבדו יחד תיענה בשנים הקרובות.
דה-צלולריזציה: לקחת איבר ולפרק רק את התאים
הטכניקה המרכזית במעבדה היא decellularization, פירוק תאי, שפותחה לראשונה ע"י Doris Taylor במינסוטה ב-2008. הרעיון פשוט: לוקחים איבר תורם (לרוב מחזיר או מאדם שלא התאים להשתלה רגילה), ושוטפים אותו בחומרים מתפרקי דטרגנטיים כמו SDS, שמסירים את כל הממברנות התאיות והדנ"א, אבל משאירים שלם את השלד התאי החוץ-תאי, אותו רשת תלת-ממדית של חלבונים שמרכיבה את המבנה של האיבר.
התוצאה היא 'איבר רפאים' שקוף, לבן, נטול תאים אבל עם כל הגיאומטריה המקורית: כלי הדם, צינוריות הכליה, התאים החיוניים של הלב. זה כמו לקבל שלד בית מוכן, מלא קומות וחדרים, רק בלי דיירים.
היתרון הגדול: השלד הזה כבר פתר את הבעיה הקשה ביותר בהנדסת רקמות, יצירת מבנה כלי דם תלת-ממדי. אי-אפשר לגדל איבר עבה בלי אספקת דם בכל נקודה, ולבנות רשת כלי דם מאפס היא משימה כמעט בלתי אפשרית. השלד הטבעי שומר על כלי הדם בצורה מושלמת, ועכשיו צריך רק להכניס תאים חדשים.
אכלוס מחדש בתאי הגזע של המטופל
השלב השני הוא recellularization, אכלוס מחדש. לוקחים תאי גזע אוטולוגיים, כלומר תאים שמקורם במטופל עצמו (לרוב iPSC, induced pluripotent stem cells, שמתוכנתים מחדש מתאי עור או דם), ומפזרים אותם דרך כלי הדם של השלד. התאים מצאים את דרכם לנישות הטבעיות שלהם, נאחזים בשלד, ומתחילים להתחלק.
סדרה של גורמי גדילה וסיגנלים כימיים מכוונת את ההתבדלות שלהם: תאי שריר לב לדפנות הלב, תאי אנדותל לכלי הדם, תאים מסוננים לכליה. בתוך 6-8 שבועות בביוראקטור, האיבר מתחיל לתפקד באופן בסיסי: הלב מתחיל לפעום, הכליה מתחילה לסנן, הכבד מתחיל לייצר אלבומין.
הביוראקטור: דמיון של גוף אנושי
הביוראקטור הוא חדר מבודד שבו האיבר 'גדל'. הוא חייב לדמות באופן מדויק את התנאים בתוך גוף האדם: טמפרטורה של 37 מעלות צלזיוס, חמצן ופחמן דו-חמצני בריכוזים פיזיולוגיים, זרימת מדיום תרבותי דרך כלי הדם בלחץ הנכון, ועד גם 'אימון' פיזי. לב, למשל, חייב 'להתאמן' מול לחץ הולך וגובר כדי לפתח שריר חזק. כליה צריכה להתאמן מול גרדיאנט אוסמולרי.
הביוראקטורים של המעבדה הקנדית הם הדור הבא: גודל של מקרר ביתי, מצוידים בעשרות חיישנים שמודדים בזמן אמת את התפקוד של האיבר, ומחוברים לבינה מלאכותית שמתאימה את התנאים אוטומטית. כל ביוראקטור עולה כ-2.5 מיליון דולר.
הראיות הנוכחיות
מחקר 1: לב חולדה מחודש מ-מינסוטה (2008)
זה היה ההוכחת היתכנות הראשונה. צוות של Doris Taylor פירק תאית לב חולדה, אכלס אותו בתאי קרדיומיוציטים חדשים, וגרם לו לפעום שוב בביוראקטור. הלב יכל לייצר 2% מהכוח של לב טבעי, מעט מאוד, אבל הוא פעם. זה היה הוכחה שהגישה אפשרית.
המחקר פורסם ב-Nature Medicine והפך לאחת הציטטות החשובות בתחום. מאז, מאות מעבדות בעולם משכפלות וקידמו את הטכנולוגיה. הלב של 2008 פעם רק כמה דקות. לבבות של 2026, באותה גישה, פועמים שבועות שלמים.
מחקר 2: כליות חזירים פונקציונליות מ-מסצ'וסטס (2022)
צוות מ-Massachusetts General Hospital פירק תאית כליות של חזירים, אכלס אותן בתאי גזע אנושיים, ושתל בחזירים. הכליות סיננו דם, ייצרו שתן, ושמרו על תפקוד 30 ימים. אמנם לא הספיק להחליף כליה אמיתית, אבל הוכח שהגישה ניתנת להרחבה לאיברים בגודל בני-אדם.
מחקר 3: לבבות חזירים בקנה מידה אנושי מטקסס (2024)
מעבדה ב-Texas Heart Institute שיחזרה לב חזיר מלא, מתאית, אכלוס בתאי iPSC אנושיים, וגידול בביוראקטור. הלב פעם בקצב של 50-65 פעימות בדקה, יצר תפוקה לבבית של 2.4 ליטר בדקה (לעומת 4-6 ליטר בלב אנושי בריא), והחזיק את התפקוד שלושה שבועות. לא מספיק להשתלה אנושית, אבל קרוב יותר מאי-פעם.
פרט קריטי: הלב לא 'נדחה' בידי המערכת החיסונית של חזירים ניסויים, כי האנדותל של כלי הדם היה אנושי. זו הוכחה ראשונית שהאסטרטגיה של 'תאי מטופל' עובדת באמת מבחינה אימונולוגית.
מחקר 4: כבד מיניאטורי שעובד 7 ימים מיפן (2025)
צוות ב-Kyoto University בנה כבד בגודל של כף יד מתאי גזע אנושיים, ושתל אותו בעכבר עם כשל כבד. הכבד המיניאטורי ייצר אלבומין ופירק תרופות במשך 7 ימים, והגדיל את הישרדות העכברים בקבוצת הניסוי ב-200%. הוא לא מחליף כבד מלא, אבל מספק 'גשר' לחולים שמחכים להשתלה.
מחקר 5: ביו-הדפסה תלת-ממדית של רקמת כליה (2025)
מעבדה ב-Wake Forest Institute for Regenerative Medicine הצליחה להדפיס מבנה כליה תלת-ממדי באמצעות ביו-הדפסת תאי גזע ומטריצה. המבנה כלל יחידות סינון פונקציונליות (nephrons) שסיננו 35% ממה שכליה אנושית בריאה מסננת. הצעד הבא: להגדיל את המבנה ולחבר לזרם דם.
מחקר 6: מערכת הביוראקטור החדשה של המעבדה הקנדית
פרסום ראשוני של המעבדה הקנדית. הם פיתחו ביוראקטור 'אדפטיבי' שמשתמש בבינה מלאכותית כדי להתאים בזמן אמת את תנאי הגידול לפי איך שהאיבר מגיב. בניסויים ראשוניים על כליות חזירים, האיברים שגדלו בביוראקטור החדש הראו תפקוד טוב פי 3 מאיברים שגדלו בביוראקטורים סטטיים.
מה עם איברים אחרים?
המעבדה הקנדית לא מתמקדת באיבר אחד. היא מתוכננת לטפל באיברים מרובים, וכל אחד עם אתגרים ייחודיים:
- כליות: יעד מספר 1. רשימת ההמתנה הארוכה ביותר, ומבנה יחסית פשוט. צפי להתחלת ניסויים בבני אדם ב-2028.
- לב: יעד מספר 2. מורכב יותר, חייב לפעום ולסנכרן תאית. צפי לניסויים ב-2030-2032.
- כבד: יעד מספר 3. הוא איבר מטבולי בעיקר, אבל הגיאומטריה שלו מורכבת ועם תאי כבד מגוונים. צפי ב-2031-2033.
- ריאות: יעד ארוך טווח. המבנה האלוויאולי עדין במיוחד וקשה לשחזר. צפי ב-2035 ואחרי.
- לבלב: יעד עתידי לחולי סוכרת מסוג 1, באמצעות גידול תאי בטא חדשים בסביבת לבלב.
- קצירה ולחיים, רקמות זעירות יותר כמו בלוטת התריס, כליות אדרנליות, ובלוטות לימפה נחשבות 'הישגים קלים' יחסית ותתאמנה ראשונה.
במקביל, המעבדה תפתח גם רקמות חלקיות, לא איברים שלמים. מחזורי שריר לב לאחר התקף לב, רקמת כבד להחלפת כבד פגום, ופלסטרים של אנדותל כליה לתיקון נזק חלקי. אלה ייכנסו לקליניקה הרבה לפני האיברים השלמים, אולי כבר ב-2027.
האם זה ריאלי, או שזה מדע בדיוני?
הריגוש לגיטימי, אבל יש סייגים חמורים שכדאי לדעת.
הפער בין מודל לבני אדם
כל המחקרים עד היום, גם המוצלחים ביותר, היו בבעלי-חיים. בני אדם הם הרבה יותר מורכבים, חיים הרבה יותר זמן, ודורשים איברים שיתפקדו עשרות שנים, לא שבועות. ייתכן שגישה שעובדת ב-3 שבועות בעכבר לא תחזיק בבן-אדם ב-30 שנה.
אתיקה של איברים כימריים
חלק מהאסטרטגיות כוללות שימוש בחיות מתחילה: למשל, גידול איבר אנושי בתוך חזיר מהונדס גנטית. זה מעלה שאלות אתיות עמוקות: האם החזיר עם מוח אנושי הוא חיה או חצי-אדם? רוב הקבוצות, כולל המעבדה הקנדית, נמנעות מהגישה הזו ועובדות עם שלדי איברים בלבד, ללא חיה חיה.
עלות אסטרונומית
גידול איבר מותאם אישית עולה הון. בערכים נוכחיים, גידול כליה מתאי המטופל עלול לעלות 800,000-1.2 מיליון דולר, יותר מהשתלת כליה רגילה. עם הזמן והרחבת הייצור, המחיר ירד, אבל יקח שנים. בישראל, סל הבריאות בודאי לא יכלול את הטיפול הזה בעשור הקרוב.
סיכון לסרטן מתאי iPSC
תאי iPSC, התאים שמתוכנתים מחדש להיות פלוריפוטנטיים, נושאים סיכון תיאורטי לסרטן. אם תא לא התבדל לחלוטין באיבר וצמח שם בקיבולת בלתי מבוקרת, הוא עלול להפוך לטרטומה, גידול שמכיל סוגי תאים מרובים. סיכון זה מטופל באמצעות בקרת איכות קפדנית, אבל לא ניתן להתעלם ממנו.
זמן הגידול הוא חסם קליני
גידול כליה לוקח 6-10 שבועות. חולה בכשל כליה חריף אין לו את הזמן הזה. הגישה הזו מתאימה לחולים עם כשל איבר כרוני שיש להם דיאליזה או טיפול גישור, אבל לא לחולים חריפים. למקרים החריפים, כליה מתורם תישאר הפתרון.
לוח זמנים ריאלי
אם הכל ילך חלק, ניסויי שלב 1 בבני אדם על כליות יתחילו ב-2028-2029. שלב 2-3 ב-2031-2033. אישור FDA, אם הכל יסתדר, לא לפני 2035-2037. ולשוק הישראלי, עוד 3-5 שנים אחרי זה.
תחרות ושיתוף פעולה
המעבדה הקנדית אינה לבד. קבוצות ב-Wake Forest, Texas Heart, Mayo Clinic, Kyoto University, ו-University of Edinburgh עובדות במקביל. סביר שתהיה תחרות, ושיתוף פעולה בינלאומי, ובסופו של דבר מאמר משולב של מי שיצליח להגיע למרפאה ראשון.
מי לא יתאים לטיפול?
גם אחרי שהטיפול יאושר, יש אוכלוסיות שלא יוכלו לקבל אותו. חולים עם הפרעות גנטיות בתאים, חולי סרטן פעיל שעלולים לפתח גידול מתאי iPSC, חולים עם דחיפות מיידית שאין להם 8-10 שבועות להמתין. מעריכים כי בערך 30-40% ממטופלי הכליות הפוטנציאליים לא יוכלו לקבל את הטיפול גם כשהוא יהיה זמין.
מה כן אפשר לעשות בינתיים?
- אם אתה ברשימת המתנה להשתלה, אל תתלה את כל התקווה בטכנולוגיה הזו. היא אכן מבטיחה, אבל תיקח 10-15 שנים להגיע לקליניקה. הטיפול הנוכחי, השתלה מתורם, נשאר הסיכוי הטוב ביותר לטווח קצר ובינוני.
- שמור על האיברים שלך בריאים. כליות, לב וכבד מגיבים מצוין לאורח חיים בריא: דיאטה ים-תיכונית, פעילות גופנית של 150 דקות בשבוע, שינה איכותית, ולא לעשן. פעולות פשוטות אלה מקטינות את הסיכוי שתצטרך השתלה ב-50-70%.
- בדוק את התפקוד הכלייתי שלך באופן שגרתי. בדיקת קריאטינין ו-GFR פעם בשנה אחרי גיל 50 יכולה לזהות בעיות מוקדם, כשעדיין יש זמן לעצור או להאט הידרדרות.
- אם יש לך מחלת כליה כרונית בשלב מוקדם, פעל עכשיו. תרופות כמו SGLT2 inhibitors (אמפליפלוזין) ו-finerenone הוכחו כמאטות הידרדרות כלייתית באופן משמעותי. שיחה עם נפרולוג היא קריטית.
- שקול לתרום איברים. גם אם הטכנולוגיה הזו תפתור את הבעיה בעתיד הרחוק, היום, אנשים מתים ברשימת ההמתנה. סימון תרומת איברים ברישוי הנהיגה או חתימה על כרטיס תורם זה מעשה שיכול להציל עד 8 אנשים אחרי המוות.
- הצטרף לרישומי מחקר רגנרטיבי בישראל. בית החולים שיבא, רמב"ם, ואיכילוב מובילים מחקר רפואה רגנרטיבית. כשניסויים קליניים יגיעו לארץ, רישומים מוקדמים יהיו הדרך הטובה ביותר להצטרף.
- הימנע מתרופות נפרוטוקסיות אם אפשר. NSAIDs (איבופרופן, נפרוקסן) במינון גבוה ולאורך זמן, אנטיביוטיקות מסוימות, וניגודיים בבדיקות הדמיה, כל אלה יכולים לפגוע בכליות בעיקר אם הן כבר חלשות.
הפרספקטיבה הרחבה
הסיפור של מעבדת התחדשות איברים אינו רק סיפור על איברים. הוא מסמן שינוי פילוסופי עמוק באופן שבו אנחנו חושבים על רפואה. עד היום, רפואה הייתה בעיקר תיקון ושימור. כשאיבר נשבר, אנחנו מנסים להאט את ההידרדרות, או במקרה הקיצוני, להחליף אותו באיבר של מישהו אחר. הגישה הרגנרטיבית פותחת אפשרות אחרת: החזרת הגוף למצב שבו הוא יכול לבנות איבר חדש משלו, כמו לטאה שמגדלת זנב חדש.
זו לא רק טכנולוגיה, זו תפיסת עולם. היא אומרת שהזדקנות וכשל איברים אינם תהליכים בלתי הפיכים, אלא מצבים שאפשר להפך אותם, אם יש לנו את הכלים הביולוגיים הנכונים. וזה משתלב באופן עמוק עם המגמה הרחבה ברפואה האנטי-אייג'ינג: יותר ויותר, אנחנו מבינים שגוף האדם הוא מערכת מתחדשת, ושמה שצריך זה לתת לה את התנאים והכלים לעשות זאת.
חשוב גם להזכיר שזה לא פתרון לכל מצב. הטכנולוגיה הזו לא תחליף תזונה בריאה, פעילות גופנית, או שינה איכותית כיסודות הבריאות. היא תהיה כלי נוסף בארגז, לא תחליף לכלים הקיימים. אדם שעוסק בכל היסודות ושומר על איברים בריאים, עשוי לעולם לא להזדקק לטיפול הזה. אדם שלא, עדיין יזדקק לתורם או לתרופות תומכות, גם אם בעתיד הוא יקבל איבר רגנרטיבי.
וגם אם הטיפול הספציפי הזה ייקח עוד 10-15 שנים להגיע למרפאות בישראל, הוא משנה את האופן שבו אנחנו צריכים לחשוב על העתיד שלנו. לא עוד 'איברים שמסיימים את חייהם עם הגוף', אלא 'איברים שיש להם שירות תחזוקה מקצועי וניתן לחדש אותם'. זו תפיסה חדשה לחלוטין של מה זה אומר להיות אנושי, ומה זה אומר לחיות חיים ארוכים ובריאים.
חשוב גם להעריך את העלות החברתית של ההגעה לכאן. מאחורי כל פריצת דרך כזו עומדים עשרות שנים של מחקר בסיסי, מיליארדי דולרים במימון, ואלפי חוקרים שעבדו על חתיכות קטנות של הפאזל. המעבדה הקנדית היא לא הישג של מעבדה אחת, אלא הצטברות של עבודה בינלאומית, שיתוף ידע, ופירסום פתוח. זה תזכורת לחשיבות של מדע פתוח ומימון ציבורי למחקר בסיסי.
ולסיום, האספקט שלא מדברים עליו מספיק: אם נצליח להפיק איברים בקלות יחסית, זה ישנה את כל הכלכלה של רפואת ההשתלות. שוק שמושג היום במחיר של 50 מיליארד דולר בשנה רק על השתלות איברים, תרופות נגד דחייה, ודיאליזה לחולים שממתינים, יעבור שינוי דרמטי. חברות תרופות שמייצרות כיום מדכאי חיסון יצטרכו להתאים את עצמן, ובתי חולים יצטרכו לשנות את המודל העסקי שלהן. זו לא רק פריצת דרך רפואית, אלא טלטלה כלכלית רחבה.
איברים שצומחים במעבדה הם, אם כך, לא רק חידוש רפואי. הם שינוי בתפיסה של מה זה אומר להזדקן, מה זה אומר להיכשל, ומה זה אומר להתחדש. זה הופך את ההתחדשות מחלום למתכון, ואת הרפואה ממקצוע של תיקון למקצוע של בנייה מחדש.
הפניות:
Hospital News - Building the World's First Organ Regeneration Lab
Google News - Original Article

💬 תגובות (0)
היו הראשונים להגיב על המאמר.