בתוך כל תא בגוף שלך יש בין 100 ל-2,000 מיטוכונדריות, איברונים זעירים שמייצרים את ה-ATP, מטבע האנרגיה של החיים. אבל מיטוכונדריות הן גם מקור הבעיה: הן דולפות רדיקלים חופשיים, ה-DNA שלהן מצטבר נזק, וכאשר הן מתקלקלות הן הופכות למזיקות יותר ממה שהן מועילות. הטבע פתר את הבעיה הזו לפני יותר מ-500 מיליון שנה עם מנגנון אלגנטי: מיטופאגיה, תהליך שבו התא מזהה מיטוכונדריות פגומות, עוטף אותן בקרום, ומפרק אותן לחלקיהן.
ב-15 במאי 2026 פרסמה The Manila Times ידיעה על מענק חדש מקרן Countdown Grant Foundation שיממן מחקר ייעודי במיטופאגיה. הקרן רואה במיטופאגיה צוואר הבקבוק של רפואת ההזדקנות: לפי המייסדים, כשל במיטופאגיה הוא הגורם המכני המוקדם ביותר לפרקינסון, מחלות לב, מחלות כליה, ותסמינים רחבים של הזדקנות בכל רקמה. הקשר בין מיטופאגיה והזדקנות הופך לאחת מהחזיתות הפעילות ביותר בביוטכנולוגיה ב-2026, עם תחרות בין חברות לפתח את ה'מגביר מיטופאגיה' הראשון שיאושר על ידי FDA.
מה זה מיטופאגיה?
המילה מיטופאגיה היא צירוף של מיטוכונדריון ו-פאגוס (לאכול ביוונית). בפועל זה תהליך שבו התא מבצע 'איסוף אשפה' ספציפי למיטוכונדריות פגומות:
- זיהוי, התא מזהה איזו מיטוכונדריה איבדה את פוטנציאל הממברנה שלה (Δψm נמוך) או צוברת נזק חמצוני.
- תיוג, חלבונים מיוחדים, בעיקר PINK1 ו-Parkin, מתיישבים על המיטוכונדריה הפגומה ומתייגים אותה בשרשרת אוביקוויטין.
- ליפוף, ממברנה כפולה (אוטופאגוזום) נסגרת סביב המיטוכונדריה המתויגת.
- פירוק, האוטופאגוזום מתמזג עם ליזוזום ואנזימים הידרוליטיים מפרקים את המיטוכונדריה.
- מחזור, החלקים נשלחים לבניית מיטוכונדריות חדשות (יחד עם תהליך הביוגנזה דרך PGC-1α).
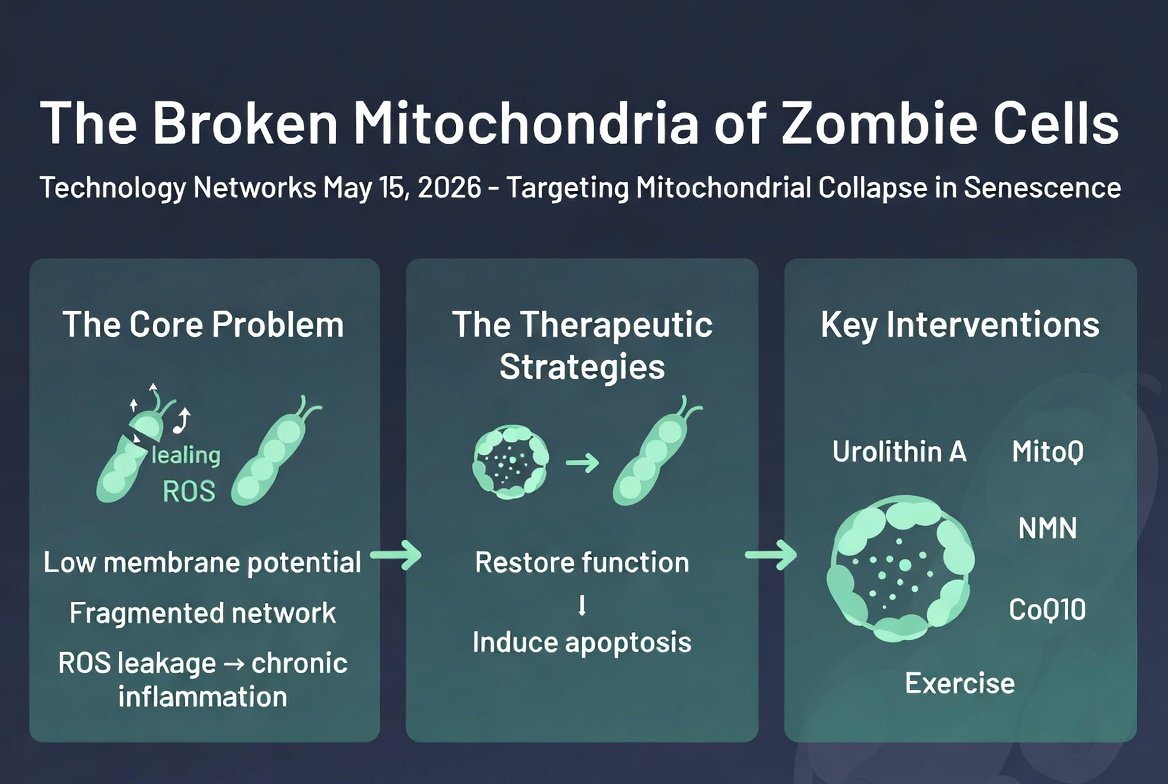
בתא צעיר, התהליך פועל ללא הרף. בערך 1-2% מהמסה המיטוכונדריאלית מתחלפת בכל יום. בתא קשיש, הקצב יורד פי 3 עד 5. התוצאה: מיטוכונדריה ישנה, פחות יעילה, ויותר מדליפה ROS.
הקשר למיטופאגיה והזדקנות: מסלול PINK1-Parkin
במרכז הסיפור עומד מסלול ביוכימי אחד שמדענים פיענחו במהלך 15 השנים האחרונות. הוא נקרא PINK1-Parkin, על שם שני החלבונים הראשיים שלו, ושימש כמקור ראשון להבנה שמיטופאגיה לקויה גורמת למחלה אנושית.
PINK1 (PTEN-Induced Kinase 1) הוא חיישן הפגם. בדרך כלל הוא נכנס למיטוכונדריה תקינה ומתפרק במהירות. אבל כשהמיטוכונדריה איבדה את הפוטנציאל הממברני שלה, PINK1 לא מצליח להיכנס פנימה, נשאר על הממברנה החיצונית, ומצטבר שם. הוא מתפקד כדגל אדום.
הדגל הזה מגייס את Parkin, אנזים מסוג E3 ubiquitin ligase. Parkin מתחיל לקבע אוביקוויטין לחלבונים על הממברנה החיצונית של המיטוכונדריה. שרשרות האוביקוויטין הללו הן ה'תווית' שאומרת למערכת האוטופאגיה: 'את האברון הזה צריך לסלק'.
גילוי המסלול הזה הגיע ממחקר פרקינסון בגיל צעיר. אנשים עם מוטציות במורשת ב-PINK1 או ב-Parkin מפתחים פרקינסון לפני גיל 40. הסיבה: נוירוני הדופאמין שלהם, שמסתמכים על מיטוכונדריות איכותיות במיוחד, צוברים מיטוכונדריות פגומות ומתים בשלב מוקדם של החיים. השמועה כי 'פרקינסון הוא מחלה של מיטופאגיה' התחילה כאן והתפשטה למחלות אחרות.
עם הגיל, גם בלי מוטציה, רמות PINK1 ו-Parkin פוחתות. מחקר רוחב ב-Cell Reports מ-2023 הראה שביטוי PINK1 במוח אדם יורד בכ-40% בין גיל 30 לגיל 70. זה אומר שגם בלי מחלה גנטית, המערכת לסילוק מיטוכונדריות פגומות הולכת ומתקלקלת באופן הדרגתי.
הראיות הנוכחיות
מחקר 1: אורוליטין A במבוגרים בריאים, Mitopure של Amazentis, 2022-2025
הניסוי הקליני הראשון בעולם של מגביר מיטופאגיה בבני אדם בוצע על ידי חברת Amazentis השוויצרית. אורוליטין A, מטבוליט שהמיקרוביום במעי מייצר מאלאגיטאנינים (תרכובות שנמצאות ברימונים ובאגוזי מלך), נמצא כמפעיל מיטופאגיה דרך מסלול PINK1-Parkin. ניסוי על 88 קשישים בגיל 65-90 שנטלו 500 או 1,000 מ"ג ביום במשך 4 חודשים הראה שיפור של 12% בכוח שריר רגליים ועלייה של 17% בסיבולת אירובית, יחד עם ירידה במדדי דלקת. המוצר משווק כיום בשם Mitopure.
מחקר 2: HIIT ומיטופאגיה, Mayo Clinic, 2025
צוות במאיו קליניק הראה שאחרי 12 שבועות של אימוני HIIT בקשישים בגילי 65-80, ביטוי הגנים של מיטופאגיה (כולל PINK1, Parkin, BNIP3) עלה בכ-65% בביופסיות שריר. במקביל, איכות המיטוכונדריות (פוטנציאל הממברנה הממוצע) השתפרה ב-30%. פעילות גופנית בעצימות גבוהה היא הממריץ הטבעי הכי חזק של מיטופאגיה הידוע לרפואה.
מחקר 3: ניסוי PINK1 בפרקינסון, אוניברסיטת לוס אנג'לס, 2024
צוות בלוס אנג'לס פיתח מולקולה קטנה (PINK1-001) שמייצבת את PINK1 על הממברנה המיטוכונדריאלית גם בנוכחות מוטציה. בעכברים עם מודל פרקינסון, המולקולה צמצמה אובדן נוירוני דופאמין ב-58% ושמרה על תפקוד מוטורי. ניסוי שלב 1 בבני אדם החל ב-2025 והתוצאות צפויות ב-2027.
מחקר 4: צום והשפעתו על מיטופאגיה, אוניברסיטת קופנהאגן, 2023
צום של 16 שעות לפחות מעלה את מדדי המיטופאגיה ב-60% בכבד ובשריר אדם, דרך אקטיבציה של AMPK ועיכוב mTOR. הסבירות הגבוהה היא שזו הסיבה שצום לסירוגין משפר תפקוד מטבולי גם ללא הפחתת קלוריות כוללת.
מחקר 5: כשל מיטופאגיה ובמחלות נדירות, NIH, 2024
סדרה של 17 מחלות מטבוליות נדירות (כולל תסמונת Leigh ותסמונת MELAS) קושרה לכשל ספציפי במיטופאגיה. בכל אחת מהן, נצפו 40-80% פחות מיטוכונדריות בהיקף ופי 3-5 יותר מיטוכונדריות מקוטעות. ה-Countdown Grant מתמקד במחלות הללו כשער כניסה לרגולציה.
מה עם מחלות לב, כליה, ומחלות כרוניות?
אחרי שהקשר למחלות נוירודגנרטיביות הובהר, החוקרים פנו לשאר הגוף. אי-ספיקת לב מתאפיינת בקרדיומיוציטים שמלאים במיטוכונדריות פגומות. מחקרים בעכברים הראו שהפעלה של מיטופאגיה מקטינה את גודל אוטם הלב ב-30%.
מחלת כליות כרונית, פגיעה במיטופאגיה בתאי הצינוריות נמצאה בכל ביופסיה מחולי כליה כרוניים. השחזור של מיטופאגיה דרך אורוליטין A במודלים מן החי האט את ההתקדמות לאי-ספיקת כליות.
סוכרת מסוג 2, תאי הלבלב המייצרים אינסולין נשענים מאוד על מיטוכונדריות. כשל במיטופאגיה גורם לתאים אלו לאבד את הרגישות לגלוקוז ולהפסיק לייצר אינסולין. תרופות חדשות שמכוונות למיטופאגיה בלבלב נמצאות בשלבי מחקר מוקדמים.
סרטן, הקשר כאן מסובך. בשלבים מוקדמים, מיטופאגיה תקינה מונעת היווצרות סרטן. אבל בשלבים מתקדמים, חלק מהגידולים נשענים על מיטופאגיה כדי לשרוד תנאי לחץ ולעמוד בפני כימותרפיה. לכן עיכוב מיטופאגיה דווקא נחקר כטיפול בסוגי סרטן מסוימים.
האם אנחנו אמורים להתחיל לקחת תוסף שמגביר מיטופאגיה?
נכון ל-2026, יש מספר אפשרויות עם רמות שונות של ראיות:
אורוליטין A (Mitopure, 500-1,000 מ"ג ליום)
הראיות הקליניות הכי טובות שיש למגביר מיטופאגיה בבני אדם. מחיר: 350-500 שקלים לחודש. מתאים במיוחד לקשישים עם חולשת שריר, סרקופניה, או חולשה כללית. תופעות לוואי קלות (אי-נוחות בקיבה ב-5-8% מהמטופלים). הסיכון העיקרי: אין נתוני בטיחות מעל שנתיים.
ספרמידין (1-3 מ"ג ליום)
פוליאמין שמופיע באופן טבעי בנבט חיטה, גבינות מיושנות, וסויה. הראיות שלו לגבי מיטופאגיה דקות יותר מאלו של אורוליטין A, אבל זה מגיע במחיר נמוך ובבטיחות מצוינת לאחר אלפי שנים של צריכה תזונתית.
NMN ו-NR (העלאת NAD+)
NAD+ דרוש למיטופאגיה תקינה. השלמת NMN מעלה NAD+ ב-30-40% ובעקיפין מעודדת מיטופאגיה. אזהרה: מחקר מ-Washington University 2024 הראה ש-NMN עשוי לעזור לתאי סרטן עמידים לשרוד טיפול. מי שיש לו גורמי סיכון לסרטן צריך להתייעץ עם רופא.
פעילות גופנית
ההתערבות הזולה ביותר עם הראיות הכי חזקות. 2-3 אימוני HIIT בשבוע מגבירים את מיטופאגיה יותר מכל מולקולה שנבדקה עד היום. ההבדל: לפעילות גופנית יש את התופעות הצדדיות הצנועות ביותר.
הסיכון בלקיחת 'מגביר מיטופאגיה' לא ממוקד
אסור לזלזל באפשרות שמיטופאגיה חזקה מדי תהיה גם בעייתית. נוירונים, למשל, מסתמכים על מיטוכונדריות שמתקיימות זמן רב יחסית. הגברת מיטופאגיה מעבר לרמה הפיזיולוגית עלולה לגרום לתאים לאבד מיטוכונדריות חיוניות. תוסף הוא לא תרופה: כדאי להתחיל במינון נמוך ולעקוב.
מה כן לעשות מהיום
- הוסף 2-3 אימוני HIIT בשבוע. הפרוטוקול הקלאסי: 4 אינטרבלים של 4 דקות בעצימות 85-95% מהדופק המקסימלי, עם 3 דקות התאוששות בין כל אחד. זה הממריץ הטבעי החזק ביותר של מיטופאגיה הידוע למדע.
- אכל רימונים, אגוזי מלך ופטל, שלוש פעמים בשבוע. הם מספקים אלאגיטאנינים, החומר הגלם שמהמיקרוביום ימיר לאורוליטין A. אצל 30-40% מהאוכלוסייה ההמרה במיקרוביום תקינה. בשאר, התוסף הישיר עדיף.
- צום של 14-16 שעות מדי יום. למשל 19:00-11:00 בבוקר. הצום מפעיל מיטופאגיה דרך AMPK ועיכוב mTOR. זוהי הדרך הזולה והטבעית ביותר להעלות את הקצב.
- שינה איכותית של 7-8 שעות. מיטופאגיה מגיעה לשיא שלה במהלך שינה עמוקה. שינה גרועה דומה לעצירת המנגנון הטבעי לסילוק מיטוכונדריות פגומות.
- שקול תוסף אורוליטין A (Mitopure או מוצר דומה) אם אתה מעל גיל 50 או עם סימני חולשת שריר. 500 מ"ג ביום במשך 4 חודשים זה הפרוטוקול הקליני שהוכח.
- אם יש בעיה משפחתית של פרקינסון, התייעץ עם נוירולוג לגבי בדיקה גנטית של PINK1 ו-Parkin. גילוי מוקדם של מוטציה לא משנה היום את הטיפול, אבל מסייע במעקב.
הפרספקטיבה הרחבה
ה-Countdown Grant מסמן רגע חשוב ברפואת ההזדקנות. במשך עשרים שנה, מיטופאגיה הייתה מושג ביולוגי מעניין שמדענים בסיסיים חקרו במעבדה. עכשיו, בעקבות הצלחת אורוליטין A בבני אדם, היא הופכת ליעד תרופתי לגיטימי שמושך השקעות של מאות מיליוני דולרים.
הרעיון העמוק יותר הוא שהזדקנות אינה מצב סטטי שצריך 'לתקן' בבת אחת, אלא תהליך דינמי של הצטברות פסולת תאית. בכל יום הגוף מייצר חלבונים פגומים, מיטוכונדריות פגומות, ותאים זומבים. כל חיים בריאים תלויים ביעילות מערכות הניקוי. כשהן עובדות, גם בגיל 80 התאים נראים יחסית צעירים. כשהן נכשלות, גם בגיל 50 כבר רואים את הסימנים.
אבל המסר החשוב ביותר נשאר עקבי: לפני שמחפשים תוסף או תרופה, יש לבדוק אם המנגנונים הטבעיים פועלים. פעילות גופנית, צום מתון, שינה ארוכה, ותזונה עשירה בפיטוכימיקלים, אלה מפעילים את אותם מסלולי מיטופאגיה שמדענים מנסים לחקות במולקולות. תרופת ההזדקנות הטובה ביותר של 2026 היא עדיין זו שאין לה פטנט.
הפניות:
The Manila Times - Countdown Grant Explores How Cells Remove Damaged Mitochondria (2026-05-15)


💬 תגובות (0)
היו הראשונים להגיב על המאמר.